|
Содержание
< назад вперед >
§ 20. ЗАКОН ФАРАДЕЯ
Фарадеем установлено, что
количество вещества, выделяющегося при электролизе на электродах,
пропорционально току и времени его прохождения, или иначе, количеству
электричества, протекающего через электролит.
Один и тот же ток, проходя
одинаковое время через различные электролиты, выделяет на электродах различное
количество вещества. Количество вещества в миллиграммах, выделяемое на электроде
током в 1 а в течение 1 сек, называется электрохимическим эквивалентом и обозначается буквой α.
Количество различных веществ,
выделяемых одним и тем же количеством электричества, пропорционально их
электрохимическим эквивалентам.
Электрохимический эквивалент
определяют опытным путем.
Ниже приведены электрохимические эквиваленты
ряда веществ:

Закон Фарадея выражается
формулой
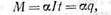
где М — количество вещества, мг;
а — электрохимический
эквивалент;
I — ток, а;
t — время, сек;
q
— количество электричества, к.
Пример 1. Определить, какое количество металлического никеля
выделит на катоде из раствора сернокислого никеля ток 5 а в течение 20 мин:
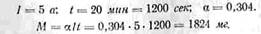
Необходимо заметить, что
количество вещества, выделяющегося при электролизе, не зависит от формы
гальванической ванны, концентрации раствора, температуры и т. п.
Содержание
< назад вперед >
| 
